Caro paziente,
questa sezione, al pari delle altre nel sito, è stata sviluppata evidenziando le domande più rilevanti che pazienti e sanitari ci hanno mosso negli anni. Vista l’importanza di questa malattia, tuttavia, e la nostra specifica dedizione all’argomento, ti proponiamo di partire da una trattazione generica, ma che riteniamo efficace su https://it.wikipedia.org/wiki/Sindrome_di_Brugada
La Sindrome di Brugada in breve: è una anomalia genetica, ovvero con la quale si nasce e che viene ereditata dai genitori e trasmessa alla discendenza. E una anomalia fatale nella maggior parte dei casi, spesso asintomatica e la sua prima manifestazione può essere la morte improvvisa, anche durante il sonno, o addirittura nella culla tanto da essere definita in passato sudden infant death. Essa può altresì manifestarsi durante attività sportiva, durante ebbre, durante l’assunzione di alcuni farmaci che ne facilitano la manifestazione e durante patologie che non riguardano il cuore. Tipicamente essa incorre in individui apparentemente sani, ovvero senza che vi sia un infarto, o particolari problematiche e quindi anche e soprattutto nei giovani. Attualmente, vista la sua natura subdola, vi è un notevole impegno da parte della comunità scientifica per la sua risoluzione, il primo riscontro, tuttavia, rimane casuale nella maggior parte dei casi, con età media intorno ai 40 anni e a seguito di un ecg (elettrocardiogramma) eseguito per differenti motivi e senza che vi sia alcun sospetto di una compromissione cardiaca. Al pari del diabete, o dell’emofilia, esistono cure efficaci nella prevenzione di morte e disabilità causate dalla Sindrome di Brugada, sebbene non esista ancora una cura per la malattia in sé. La sua prevalenza media è dello 0,10%, ovvero di una persona ogni 1000 abitanti: ipotizzando che un centro specialistico svolge 1000 ecg a settimana quindi l’incidenza di un ecg sospetto è quindi molto elevata.
Quali sono i meccanismi molecolari/cellulari della malattia?
Una anomalia genetica causa la sintesi di proteine anomale che impediscono il passaggio degli ioni sodio nelle cellule del cuore. Tali ioni sono indispensabili alla trasmissione degli impulsi elettrici per la contrazione del muscolo cardiaco e questa anomalia provoca aritmie ventricolari mortali.
Quando si manifesta prevalentemente la malattia, ovvero quando un Brugada è più a rischio di morire?
In stati di riposo e durante il sonno, o a seguito di assunzione (spesso causale) di farmaci come la flecainide (almarytm, fleiderina), o gli anti depressivi triciclici.
Chi diagnostica e cura la Sindrome di Brugada?
L’aritmologo, ovvero il cardiologo particolarmente esperto in diagnosi e cura delle aritmie e che ha una preparazione specifica anche in genetica cardiovascolare.
Serve uno specialista in genetica per la Sindrome di Brugada?
No, solo un aritmologo preparato.
Quale è il primo sospetto, anche in un paziente asintomatico?
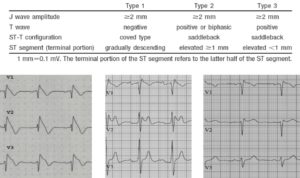
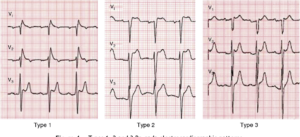
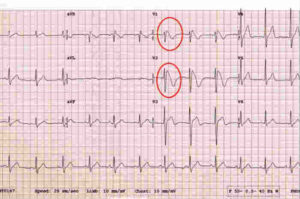
All’esame elettrocardiografico di base (ECG) si nota un ritardo di conduzione intra ventricolare destro e prevalente in V1 e V2 associato ad un tipico sopra-slivellamento del tratto ST.
Che si deve fare se vi è il sospetto di una Sindrome di Brugada in qualsiasi età? Insomma come si svolge esattamente la diagnosi?
In presenza di un ecg basale sospetto, con o senza una storia di morte improvvisa familiare, il paziente deve sottoporsi ad un test alla flecainide o alla ajimalina e ad analisi genetiche. Per la diagnosi servono infatti solo questi banali elementi: visita aritmologica, ecg, test farmacologico non invasivo e genetica. Dopo la diagnosi, tuttavia, va stratificato anche il rischio che la sindrome porta, per poter pianificare gli interventi terapeutici volti a non far morire questo paziente e i suoi parenti.
Che si fa quindi dopo la diagnosi?
Si stratifica il rischio in 3 classi mediante un test da sforzo, uno o più holter ecg delle 24 ore ed uno studio elettrofisiologico endocavitario. Vanno inoltre valutati con visita aritmologica, ecg e esami genetici tutti i consanguinei diretti in vita.
Che si fa in caso di una diagnosi positiva?
In classe di rischio 1 e 2 ci si limita ad una stretta osservazione e alcune limitazioni comportamentali, in classe di rischio 3 si opera il paziente impiantando il defibrillatore (ICD) trans-venoso, o sottocutaneo. Dal 2019 è possibile anche accedere ad un intervento di ablazione ancora in via sperimentale.
Come si cura la Sindrome di Brugada?
Attualmente non si cura: i presidi che utilizziamo servono a resuscitare il paziente in caso di aritmia maligna e consistono in due tipi di defibrillatori impiantabili, il trans-venoso ed il sottocutaneo. Esiste inoltre un intervento sperimentale di ablazione, ma è in fase di studio e con certezza non provata a lungo termine, ovvero valutato su un ristretto numero di pazienti, da un ristretto numero di operatori e per un ristretto lasso di tempo. Tale intervento è da noi praticato, ma riservandolo a chi ha già un ICD impiantato, ovvero in un doppio intervento (ablazione + defibrillatore), ovvero senza negare la possibilità del defibrillatore semiautomatico ad un paziente con un rischio di morte elevato fino al momento in cui la terapia con ablazione non sarà comprovata come efficace.
Vale la pena indagare e poi curare la sindrome di Brugada anche ad un paziente non più giovane, piuttosto che francamente anziano?
Assolutamente sì, poiché un paziente ammalato, a qualsiasi età, svela una tara genetica e familiare che probabilmente affligge, o affliggerà tutti i suoi parenti. Svelare la malattia in un qualsiasi paziente significa salvare tempestivamente gli altri consanguinei e del resto non vi deve essere alcun limite di età per praticare una buona medicina.
Come si svolgono gli esami che permettono al diagnosi? In che luogo ed in che tempo? A quale costo?
Si tratta di esami diagnostici di primo secondo e terzo livello, di breve durata, non invasivi, disponibili per tutti e convenzionati con il sistema sanitario nazionale. Essi si svolgono in ambulatorio di aritmologia ad esclusione dei test farmacologici che si svolgono in Day Hospital in una struttura di alta specialità cardiologica. Per accelerare i tempi, ovvero ridurre i rischi dovuti ad un ritardo diagnostico e terapeutico, viene spesso proposto un ricovero ordinario di due notti per svolgere sia i test farmacologici che fanno diagnosi che lo studio elettrofisiologico endocavitario che partecipa alla stratificazione del rischio post diagnosi.
